【日本】パテントリンケージにおいて不正競争行為該当性(不正競争防止法2条1項21号)が争われた事例
東京地裁令和7年10月29日判決(令和7年(ワ)第70139号)
1.事件の概要
被告(バイエル薬品)は業界紙への謹告(以下「本件謹告」という。)の掲載及び厚生労働省(以下「厚労省」という。)に対する回答(以下「本件回答」という。)において、原告(日本ジェネリック)の医療用後発医薬品の製造販売行為が本件特許権(特許第4143297号)を侵害する旨の流布・告知を行った。
本件は、原告が、被告による業界紙への謹告の掲載及び厚労省に対する回答が、不正競争防止法(以下「不競法」という。)2条1項21号所定の不正競争(虚偽の事実の流布・告知)に当たると主張して、同法3条1項に基づく差止め及び同法14条に基づく信用回復措置を求めた事案である。
東京地裁は、本件謹告及び本件回答が、「他人の営業上の信用を害する」(不競法2条1項21号)ものであるとはいえないことを理由として、原告の請求を棄却した。
2.事件の経緯
被告は、平成24年4月から、リバーロキサバンの普通錠、及びリバーロキサバンのOD錠や細粒分包(以下、これらを「被告製品等」という。)を製造販売している。
このような状況下で被告は、令和2年12月4日から令和6年7月29日まで6回にわたり、業界紙である日刊薬業に「リバーロキサバンに関する特許権について」と題する謹告を掲載した。
原告は、令和5年2月、厚生労働大臣に対し、被告製品等の医療用後発医薬品(以下「後発医薬品」という。)について、薬機法14条1項所定の製造販売の承認申請をし、令和6年8月、上記承認申請につき、「効能又は効果」を「非弁膜症性心房細動患者における虚血性脳卒中及び全身性塞栓症の発症抑制」とする限度で、製造販売の承認を受けた。
厚労省及び独立行政法人医薬品医療機器総合機構(以下「PMDA」といい、厚労省と併せて「厚労省等」という。)は後発医薬品の薬機法上の承認審査に当たり後発医薬品の安定供給を確保する観点から、既承認の医療用医薬品(以下「先発医薬品」という。)の有効成分に係る物質特許又は用途特許についての情報収集等を行い、後発医薬品について、先発医薬品に係る特許との抵触の有無を確認している。この過程において、厚労省は特許権者等である被告に説明を求め、回答(以下「本件回答」という。)を得ている。
原告は、本件謹告の掲載が「他人の営業上の信用を害する虚偽の事実」を流布するものであり(争点1)、また本件回答が「他人の営業上の信用を害する虚偽の事実」を告知するものである(争点2)として、東京地裁に訴えた。
3.パテントリンケージとの関係
厚労省等は、後発医薬品の薬機法上の承認審査に当たり、厚労省の通知(「承認審査に係る医薬品特許情報の取扱いについて」(平成6年10月4日薬審第762号厚生省薬務局審査課長通知。以下「平成6年通知」という。)及び「医療用後発医薬品の薬事法上の承認審査及び薬価収載に係る医薬品特許の取扱いについて」(平成21年6月5日医政経発第0605001号、薬食審査発第0605014号厚生労働省医政局経済課長・厚生労働省医薬食品局審査管理課長通知。以下「平成21年通知」という。))に基づき、後発医薬品の安定供給を確保する観点から、先発医薬品の有効成分に係る物質特許又は用途特許についての情報の収集等を行い、後発医薬品について、先発医薬品に係る特許との抵触の有無を確認している。これはTPPにおいて締約国に採用を義務付けられたものであり、「パテントリンケージ」などともいう。また、厚労省等は平成6年通知及び平成21年通知は、先発医薬品の有効成分に係る物質特許又は用途特許(特許期間が満了しているものを除く。)の特許権者(出願人)又は当該特許に係る成分を有効成分として医薬品の承認を取得している者(以下「先発医薬品の特許権者等」という。)に対し、医薬品特許情報報告票に必要事項を記入し、PMDAに提出することを求めている。ただし、先発医薬品の特許権者等による医薬品特許情報報告票の提出は任意であり、一般に公開しないものとされている。
厚労省は、原告製品の承認審査の過程で、前記の各通知に基づき、先発医薬品の特許権者等である被告に説明を求めた。本件回答は、これに対し、被告が回答したものである。
4.本件特許権及び存続期間の延長登録
ア 本件特許権
本件特許の特許権者は、バイエルグループに属するドイツ法人である。
本件特許の特許請求の範囲は、請求項1の【化1】で示される化合物であり、「リバーロキサバン」ということがある。
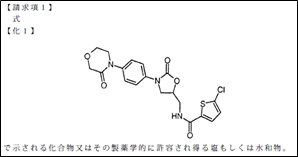
イ 本件特許権の存続期間の延長登録
本件特許権は、「10件の存続期間の延長登録出願がされ、平成25年3月21日から令和3年3月10日までに、その延長登録がされた(以下、各延長登録を同別紙の番号に対応させて「本件延長登録1」などといい、これらを「本件延長登録」と総称する。また、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律については、関係法令等で引用されている場合を除き、同改正の前後を通じて「薬機法」という。)。」ことと、本件延長登録は、「いずれもリバーロキサバンを有効成分とする医薬品(以下、剤型と対応させて「リバーロキサバンの普通錠」などということがある。)を特許法67条2項の政令で定める処分(政令処分)の対象とする。」ものである。
このうち、特定された用途を「深部静脈血栓症及び肺血栓塞栓症の治療及び再発抑制」(以下「本件用途1」という。)とする普通錠についての延長登録(本件延長登録3及び4)の存続期間は、令和7年12月11日までである」としている。
他方、「特定された用途に本件用途1を含むその余の延長登録(①特定された用途を本件用途1とする細粒分包についての延長登録(本件延長登録7及び8)、及び②特定された用途を本件用途1及び「非弁膜症性心房細動患者における虚血性脳卒中及び全身性塞栓症の発症抑制」(以下「本件用途2」という。)とするOD錠についての延長登録(本件延長登録9及び10))の存続期間は、原告製品の製造販売の申請がされた令和5年2月より前に、満了している」とされている。
5.裁判所の判断
ア 争点1(本件謹告の掲載が「他人の営業上の信用を害する虚偽の事実」を流布するものか)について
裁判所は、「本件謹告は、要旨、①被告は、リバーロキサバンを有効成分とする製品を保護する特許として、本件特許権を含む5件の特許権を保有し、本件特許権を含む3件については、それぞれの製品の承認に基づき延長登録を取得済み又は出願中であって、これらの特許権(存続期間の延長に係る部分を含む。)を侵害する行為又は侵害するおそれのある行為に対し、厳正かつ厳格なる法的処置を講じる所存であること、②リバーロキサバンを有効成分とする製品の製造、販売、輸入等を計画されている企業は、被告の知的財産権の侵害行為のなきよう十分留意してほしいことを内容とするものであり、原告製品に言及していないばかりか、侵害品たり得る製品の剤型や用途等の構成にも言及していない」とし、「業界紙に掲載された本件謹告の読者は同業者を含む製薬業の関係者であると認められるところ、本件延長登録によって本件特許権の存続期間(当初は令和2年12月11日)が延長されたことからすると、上記のような内容の本件謹告を業界紙に掲載することで同業者に対する情報提供や注意喚起を図ることは、先発医薬品メーカーとして、後発医薬品の製造販売等による特許権侵害を防止する上で自然な対応であったと考えられる」とした。
そして、「読者の普通の注意と読み方とを基準にした場合に、本件謹告は、リバーロキサバンを有効成分とする後発医薬品の製造販売行為について、剤型や用途等を含むその構成によっては、先発医薬品についての本件特許権を侵害することがあり得るという当然の事項を前提に、被告がリバーロキサバンに係る特許権を侵害する行為等には権利を行使する方針であることを一般的に述べることによって、情報提供ないし注意喚起したものと理解するというべきであり、原告製品を含む特定の後発医薬品との関係での本件特許権の権利範囲についての見解を示すものと理解するとは考え難い」と判断し、裁判所は、本件謹告が、「他人の営業上の信用を害する」(不競法2条1項21号)ものであるとはいえないと判示した。
イ 争点2(本件回答が「他人の営業上の信用を害する虚偽の事実」を告知するものか)について
裁判所は、不競法2条1項21号の「営業上の信用」とは、「取引社会における事業者の経済的価値に対する社会的評価であって、当該事業者と取引を行うかの意思決定に影響を与え得るものをいうと解するのが相当である」と判示した。そして、医薬品の製造販売の承認は、「厚生労働大臣が、医薬品等の品質、有効性及び安全性の確保並びにこれらの使用による保健衛生上の危害の発生及び拡大の防止のために必要な規制として、薬機法により与えられた権限と責任に基づいてする行政処分であって、自由競争が行われる取引社会における取引とは性質が異なる」としたうえで、「厚労省等が、後発医薬品の承認審査に当たり、先発医薬品と後発医薬品との特許抵触の有無を確認するため、必要に応じて、先発医薬品の特許権者等に補足説明を求めることは、行政処分に先立つ情報収集行為であって、そこでは、厚労省等において、後発医薬品の申請者の経済的価値に対する社会的評価を形成することが想定されているとはうかがわれない」こと、また、「厚生労働大臣は、後発医薬品の承認審査において、先発医薬品の特許権者等からの提供情報だけでなく、諸般の事情を総合考慮し、自らの権限と責任においてその判断をするものである上に、先発医薬品の特許権者等から提供される情報は一般に公開しないとされているのであるから、同情報が市場に伝ぱして取引社会における申請者の経済的価値に関する社会的評価が低下するおそれがあるということもできない」ことを理由に、本件回答をして情報提供することは、「他人の営業上の信用を害する」(不競法2条1項21号)ものであるとはいえないと判示した。
ウ 結論
裁判所は、その他の争点について判断することなく、原告の請求を棄却した。
6.コメント
ア 争点1(本件謹告の掲載が「他人の営業上の信用を害する虚偽の事実」を流布するものか)について
本判決では、業界紙への謹告について、「原告製品に言及していない」、「侵害品たり得る製品の剤型や用途等の構成にも言及していない」とし、「読者の普通の注意と読み方とを基準」にして、「特許権を侵害する行為等には権利を行使する方針であることを一般的に述べる」ものであると判断して、不正競争該当性を否定した。このように、特許権侵害の可能性について警告をすること自体は、不正競争に該当しない点について、業界紙の内容や読者の立場を考慮して判断している点は、実務上、参考になる。
なお、裁判所が判断を示す前に特許権侵害の告知又は流布する行為の違法性については、最近では、東京地裁令和7年10月9日判決(令和6年(ワ)第70096号[本訴事件]・令和6年(ワ)第70274号[反訴事件])において、「競業者が知的財産権を侵害していないにもかかわらず、その権利者において当該競業者が当該知的財産権を侵害する旨告知し又は流布する行為が、知的財産権の正当な権利行使の一環としてなされたものと認められる場合には、知的財産権の重要性に鑑み、違法性を欠くものというべきである。」と判示されている。
イ 争点2(本件回答が「他人の営業上の信用を害する虚偽の事実」を告知するものか)について
本判決では、「営業上の信用」とは、「取引社会における事業者の経済的価値に対する社会的評価」であると解釈し、厚労省による行政処分について、「自由競争が行われる取引社会における取引とは性質が異なる」と判断したうえで、先発医薬品の特許権者等による厚労省への回答は、「行政処分に先立つ情報収集行為」であって、「後発医薬品の申請者の経済的価値に対する社会的評価を形成するもの」ではなく、また、「先発医薬品の特許権者等から提供される情報は一般に公開しない」ことから、「経済的価値に関する社会的評価を低下させるもの」でもないと判示した。その結果、本件回答の不正競争該当性が否定されており、本判決により、行政への適切な回答は、不正競争に該当しにくい傾向が示された点に意義がある。
本判決における本件回答の考え方は、「アイリーア事件」(知財高裁令和7年8月13日決定(令和7年(ラ)第10003号))で判示された考え方を採用したものであるといえる。特に、行政(厚労省等)への情報提供を「信用毀損」の射程外に置く考え方がほぼ同型である。今後とも、このような考え方が定着するか否かについて、今後の裁判例の動向に注視する必要がある。
なお、パテントリンケージ制度は、現在、厚労科研において、運用改善や制度改正の可能性について調査研究が行われている。今後のパテントリンケージの制度改正の動向にも注意が必要である。
(加藤 浩)
知財高裁HP:令和7年(ワ)第70139号