【日本】特許権の存続期間の延長登録の無効審決の一部を取り消した知財高裁判決「止痒剤事件」
知財高裁 令和3年3月25日判決(令和2年(行ケ)第10098号)
1.事件の概要
本件は、発明の名称を「止痒剤」とする発明に係る特許権(特許第3531170号)について、特許権の存続期間の延長登録を無効とした審決(無効2020-800004号)の取消訴訟である。争点は、(1)審判に参加していた参加人の審決取消訴訟における被告適格の有無、(2)本件発明を実施するために、薬機法14条の処分(本件処分)を受けることが必要であったか否か、(3)延長登録の一部について無効理由があった場合に、延長登録の一部のみを無効にすることができるか否かである。
判決では、被告適格を認めた上、本件発明の実施に本件処分を受けることが必要であった上、延長登録の一部のみを無効にすることもできるとして、審決の一部を取り消した。
2.本件発明
本件審決が対象とした本件特許(請求項の数:36)のうち、請求項1に記載された発明(本件発明1)は、以下のとおりである。
【請求項1】
下記一般式(I)
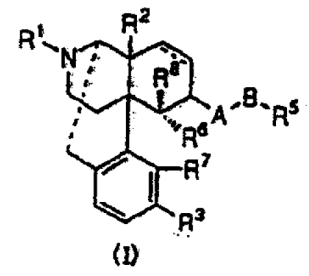
[式中,・・・]で表されるオピオイドκ受容体作動性化合物を有効成分とする止痒剤。
3.本件処分
本件の延長登録出願(2017-700310)は、販売名を「レミッチOD錠2.5μg」とする医薬品(本件医薬品)についての製造承認に基づくものであり、本件処分は、以下のとおりである。
<本件処分>
ア 延長を求める期間:5年
イ 延長登録の理由となる処分:薬機法14条9項に規定する医薬品に係る同項の承認
ウ 処分を特定する番号 22900AMX00538000
エ 処分を受けた日:平成29年9月22日
オ 処分の対象となった医薬品:販売名 レミッチOD錠2.5μg
(有効成分:ナルフラフィン塩酸塩)
カ 処分の対象となった医薬品について特定された用途
(補正前)
次の患者におけるそう痒症の改善(既存治療で効果不十分な場合に限る)
透析患者,慢性肝疾患患者
(補正後)
次の患者におけるそう痒症の改善(既存治療で効果不十分な場合に限る)
透析患者(血液透析患者を除く),慢性肝疾患患者
4.審査部における審査経緯
本件医薬品については、本件処分に先立ち、平成29年3月30日に先行処分がされていたところ、先行処分における効能・効果は、次のとおりであった。
<先行処分>
効能・効果
次の患者におけるそう痒症状の改善(既存治療で効果不十分な場合に限る)
血液透析患者、慢性肝疾患患者
本件の延長登録出願は、審査の過程で、「処分の対象となった医薬品について特定された用途」のうち、血液透析患者を対象とする部分は、先行処分に包含されるものであるとする拒絶理由通知を受けた。このため、「処分の対象となった医薬品について特定された用途」は、「透析患者(血液透析患者を除く)、慢性肝疾患患者」に補正され,平成30年7月25日、延長の期間を「5年」とする本件延長登録がされた。
5.審判部の判断
被告(沢井製薬)は,令和2年1月23日、原告(東レ)による本件延長登録について無効審判(無効2020-800004号)を請求し、被告(ニプロ)は、同年4月10日、特許法148条1項に基づく参加申請をし、特許庁は、同年6月11日、参加を許可する決定をした。審決は、以下のとおりである。
(1) 本件医薬品の有効成分の認定
本件医薬品の有効成分は,本件処分の対象となった医薬品の有効成分の記載、「医薬品インタビューフォーム」及び「添付文書」から、「ナルフラフィン塩酸塩」である。
本件発明に係る「止痒剤」は,一般式(I)で表される化合物(ナルフラフィン)を有効成分とするものであって,本件明細書の記載、及び、審査経緯からみて、一般式(I)の化合物は、塩の付加していない化合物を意味すると解するべきである。
したがって、ナルフラフィン塩酸塩を有効成分とする本件医薬品は,本件発明の発明特定事項を備えていないから,本件発明の実施に本件処分を受けることが必要であったとは認められない。
(2) 延長登録の「用途」の一部の無効
慢性肝疾患患者を対象とする場合については,先行処分によって実施できるようになっていたのであるから,慢性肝疾患患者を対象とする場合の実施に本件処分を受けることが必要であったとは認められない。
よって、本件延長登録のうち「処分の対象となった医薬品について特定された用途」が「慢性肝疾患患者におけるそう痒症の改善(既存治療で効果不十分な場合に限る)」の部分について理由がある。
(3) むすび
以上のとおり、本件延長登録は、その全体について無効とすべきものである。
6.知財高裁の判断
本判決では,被告適格を認めた上、本件発明の実施に本件処分を受けることが必要であった上、延長登録の一部のみを無効にすることもできるとして、審決の一部を取り消した。
(1) 無効審判の参加人の被告適格
特許法148条1項は、「第132条第1項の規定により審判を請求することができる者は、審理の終結に至るまでは、請求人としてその審判に参加することができる。」として、特許法148条1項に基づく参加人(以下、「1項参加人」という。)が、特許無効審判又は延長登録無効審判に「請求人」として参加することを明記している。したがって、1項参加人は、特許法179条1項の「請求人」として、被告適格を有するものと解される。
また、1項参加をすることができるのは無効審判を請求できる者に限られ、かつ、1項参加人は、特許法148条4項のような規定がなくても、当然に一切の審判手続をすることができるとされている上、被参加人が請求を取り下げても審判手続を続行できるとされている(148条2項)。これらのことは、1項参加人が、正に「請求人」としての地位を有することを示しており、そのことからしても、1項参加人は被告適格を有するものと解することができる。
なお、被告(ニプロ)に被告適格があることについては、中間判決として示されている(知財高裁令和2年12月2日中間判決(令和2年(行ケ)10098号)。
(2) 本件医薬品の有効成分の認定
特許権の存続期間の延長登録の制度の趣旨を踏まえると、本件処分の内容の認定は、実質的に判断されるべきであって、薬機法14条の承認書の「有効成分」の記載内容から形式的に判断すべきではない。また、このように解することは、最高裁平成26年(行ヒ)第356号(平成27年11月17日判決)「アバスチン事件」の趣旨にも沿うものである。
医薬品化合物において塩の形態を取る意義,当業者の認識、製造販売承認に当たってされた試験の内容、添付文書やインタビューフォームの記載などを考え併せると、本件処分の対象となった医薬品(本件医薬品)の有効成分は、先行処分に係る製造販売承認書に記載された「ナルフラフィン塩酸塩」と形式的に決するのではなく、実質的には、本件医薬品の承認審査において、効能、効果を生ぜしめる成分として着目されていたフリー体の「ナルフラフィン」と、本件医薬品に配合されている、その原薬形態の「ナルフラフィン塩酸塩」の双方であると認めるのが相当である。
したがって、「ナルフラフィン塩酸塩」のみを本件医薬品の有効成分と解し、「ナルフラフィン」は、本件医薬品の有効成分ではないと認定して、本件発明の実施に本件処分を受けることが必要であったとはいえないと判断した審決の認定判断は誤りである。
(3) 延長登録の「用途」の一部のみを無効にすることができるか否か
慢性肝疾患患者を対象とする場合については、先行処分により既に実施可能となっていたのであるから、慢性肝疾患患者を対象とする場合の実施について、本件処分を受けることが必要であったとはいえないことは明らかである。本件延長登録のうち、「用途」を「慢性肝疾患患者を対象とするそう痒症の改善」とする部分について、本件延長登録はその一部に無効理由がある。
延長登録の一部について無効理由がある場合、延長登録を全体として不可分と解して無効とすべき根拠はなく、延長登録がされた「用途」の一部について、旧特許法67条2項の政令で定める処分を受けることが必要であったとは認められない場合には、その部分のみを無効審判において無効にすることができ、そのようにすべきであると解される。
審決においては、「用途」を「慢性肝疾患患者を対象とするそう痒症の改善」とする部分が先行処分によって既に実施できるようになっていたことに基づいて、本件延長登録の一部のみを無効にしたものと解され、本件審決のこの判断は,正当なものとして是認することができる。
7.コメント
(1) 無効審判の参加人の被告適格
本判決により、延長登録無効審判に参加していた参加人は、審決取消訴訟における被告適格を有することが示された。
特許法179条1項は、被告適格に関して、延長登録無効審判のほか、特許無効審判や再審についても同様に規定しているところ、特許法148条1項において、延長登録無効審判だけでなく、特許無効審判についても、その参加人はその審判に請求人として参加できることが規定され、また、特許法171条1項において、確定審決の参加人は、再審を請求できることが規定されている。
したがって、本判決により示された「参加人の被告適格」は、延長登録無効審判だけでなく、特許無効審判や再審の審決取消訴訟にも適用されるものと考えられる。今後は、審決取消訴訟の請求も視野に入れて、これらの審判事件への参加について検討することが重要である。
(2) 本件医薬品の有効成分の認定
本判決では、本件処分の内容の認定は、実質的に判断されるべきであって、薬機法14条の承認書の「有効成分」の記載内容から形式的に判断すべきではないことが示された。
現行の特許・実用新案審査基準第IX部第2章2.4には、願書の記載事項に関して、「処分の対象となった物、及び、その処分においてその物の使用される特定の用途が定められている場合にあってはその用途を記載する」とされ、用途については、「医薬品の場合は、承認書に記載された効能・効果」を記載することとされている。
また、同じく審査基準第IX部第2章3.1.1には、審査に関して、「特許発明における発明特定事項と医薬品類の承認書又は農薬の登録票等に記載された事項とを対比した結果、本件処分の対象となった医薬品類又は農薬が、いずれの請求項に係る特許発明についてもその発明特定事項の全てを備えているといえない場合は、審査官は、拒絶理由を通知する」と規定されている。しかしながら、承認書等の記載内容から、どの程度、実質的な判断をするべきかについては、審査基準に示されていない。
今後は、本判決により、薬機法14条の承認書の「有効成分」の記載内容から、どの程度、実質的な判断がなされるのかについて、延長登録出願の審査の動向に注意が必要である。また、延長登録の判断について予見可能性を高めるには、さらなる判例の蓄積も必要であり、今後の判例の動向に注目したい。
(3) 延長登録の「用途」の一部のみを無効にすることができるか否か
本判決では、延長登録がされた「用途」の一部について、政令で定める処分を受けることが必要であったとは認められない場合には、その部分のみを無効審判において無効にすることができることが示された。とくに、延長登録の一部について無効理由がある場合、延長登録を全体として不可分と解して無効とすべき根拠はないことが示された。
今後は、特許権の存続期間の延長登録の実務において、複数の「用途」がある場合には、それぞれの用途ごとに、延長登録の要件の充足性を検討することが重要である。
8.関連事件
本件特許(特許3531170号)については、延長登録出願又は延長登録の拒絶審決又は無効審決に関して、以下の4件の各判決が同日(令和3年3月25日)に示されている(いずれも審決の取消し)。
(A)知財高裁令和2年(行ケ)10063号
下記処分(薬機法14条)に基づく延長登録出願(2017-700154)の拒絶審決(不服2018-7539号)に対する審決取消訴訟
(1)処分の対象となった医薬品
販売名 レミッチOD錠2.5μg
有効成分 ナルフラフィン塩酸塩
(2)処分の対象となった医薬品について特定された用途
次の患者におけるそう痒症の改善(既存治療で効果不十分な場合に限る)
血液透析患者,慢性肝疾患患者
(B)知財高裁令和2年(行ケ)10096号
下記処分(薬機法14条)に基づく延長登録(2015-700061)の無効審決(無効2020-800002号)取消訴訟
(1)処分の対象となった医薬品
販売名 ノピコールカプセル2.5μg
有効成分 ナルフラフィン塩酸塩
(2)処分の対象となった医薬品について特定された用途
慢性肝疾患患者におけるそう痒症の改善(既存治療で効果不十分な場合に限る)
(C)知財高裁令和2年(行ケ)10097号
下記処分(薬機法14条)に基づく延長登録(2017-700309)の無効審決(無効2020-800003号)の取消訴訟
(1)処分の対象となった医薬品
販売名 レミッチカプセル2.5μg
有効成分 ナルフラフィン塩酸塩
(2)処分の対象となった医薬品について特定された用途
次の患者におけるそう痒症の改善(既存治療で効果不十分な場合に限る)
透析患者(血液透析患者を除く)、慢性肝疾患患者
(D)知財高裁令和2年(行ケ)10098号【本件の判決】
下記処分(薬機法14条)に基づく延長登録(2017-700310)の無効審決(無効2020-800004号)の取消訴訟
(1)処分の対象となった医薬品
販売名 レミッチOD錠2.5μg
有効成分 ナルフラフィン塩酸塩
(2)処分の対象となった医薬品について特定された用途
次の患者におけるそう痒症の改善(既存治療で効果不十分な場合に限る)
透析患者(血液透析患者を除く)、慢性肝疾患患者
知財高裁HP:令和2年(行ケ)第10098号判決文
<関連条文>
<特許法>
第67条(存続期間)
4 第1項に規定する存続期間(・・・)は、その特許発明の実施について安全性の確保等を目的とする法律の規定による許可その他の処分であって当該処分の目的、手続等からみて当該処分を的確に行うには相当の期間を要するものとして政令で定めるものを受けることが必要であるために、その特許発明の実施をすることができない期間があつたときは、五年を限度として、延長登録の出願により延長することができる。
第67条の7(存続期間の延長登録)
1 審査官は、第67条第4項の延長登録の出願が次の各号のいずれかに該当するときは、その出願について拒絶をすべき旨の査定をしなければならない。
一 その特許発明の実施に第67条第4項の政令で定める処分を受けることが必要であつたとは認められないとき。
第132条(共同審判)
同一の特許権について特許無効審判又は延長登録無効審判を請求する者が二人以上あるときは、これらの者は、共同して審判を請求することができる。
第148条(参加)
1 第132条第1項の規定により審判を請求することができる者は、審理の終結に至るまでは、請求人としてその審判に参加することができる。
2 前項の規定による参加人は、被参加人がその審判の請求を取り下げた後においても、審判手続を続行することができる。
3 審判の結果について利害関係を有する者は、審理の終結に至るまでは、当事者の一方を補助するためその審判に参加することができる。
4 前項の規定による参加人は、一切の審判手続をすることができる。
第171条(再審の請求)
1 確定した取消決定及び確定審決に対しては、当事者又は参加人は、再審を請求することができる。
第179条(被告適格)
前条第1項の訴えにおいては、特許庁長官を被告としなければならない。ただし、特許無効審判若しくは延長登録無効審判又はこれらの審判の確定審決に対する第171条第1項の再審の審決に対するものにあっては、その審判又は再審の請求人又は被請求人を被告としなければならない。
<薬機法>
第14条(医薬品、医薬部外品及び化粧品の製造販売の承認)
1 医薬品(厚生労働大臣が基準を定めて指定する医薬品を除く。)、医薬部外品(厚生労働大臣が基準を定めて指定する医薬部外品を除く。)又は厚生労働大臣の指定する成分を含有する化粧品の製造販売をしようとする者は、品目ごとにその製造販売についての厚生労働大臣の承認を受けなければならない。
9 厚生労働大臣は、第一項の承認の申請があつた場合において、申請に係る医薬品、医薬部外品又は化粧品が、既にこの条又は第十九条の二の承認を与えられている医薬品、医薬部外品又は化粧品と有効成分、分量、用法、用量、効能、効果等が明らかに異なるときは、同項の承認について、あらかじめ、薬事・食品衛生審議会の意見を聴かなければならない。